仅搜集收录了部分个人感兴趣的文章,并进行简单记录
1 概念科普
1.1 人工智能有利于 ICU 的血流动力学管理
2025年01月03日 17:54 文章链接
优化当前的血流动力学监测
- 无创监测:基于 AI 的热成像可以预测休克,从而改善资源管理和患者体验
- 监测设备增强:分析单导联心电图数据的深度神经网络可以检测升高的左心房压并估计左心室射血分数。对于侵入性监测,人工智能驱动的脉搏轮廓分析从动脉波形中提取每搏输出量 (SV),性能优于传统方法
- 解决心血管难题:根据血压、近红外光谱 (NIRS) 脑氧合和经颅多普勒 (TCD) 血流速度等数据训练的支持向量机在预测低血容量方面显示出前景
预测血流动力学恶化
- 低血压预测指数 (HPI) 等算法可以通过分析动脉波形来预测低血压,由于代偿机制,动脉波形可能保持稳定
血流动力学状况的分类或特征
- AI 有助于对患者和疾病进行分类,例如区分动脉颤动和窦性心律
- AI 模型甚至可以预测心律失常的发作,为先发制人的干预铺平道路
- 主动脉瓣狭窄 (AoS) 是另一种可以从 AI 驱动的分类中受益的疾病。AoS 通常通过经胸超声心动图 (TTE) 进行诊断,但使用血压波形的 AI 模型可以无创地检测到它,具有很高的准确性
- AI 也用于对休克和低血压内型进行分类。例如,分层聚类确定了 6 种不同的术中低血压内型,为量身定制的治疗方法提供了见解
治疗支持
- 血流动力学稳定指数 (HSI) 通过分析 ICU 数据来预测重症患者的不稳定情况,AUC 为 0.82,特异性为 92%
- AI 还支持特定的治疗方法,如液体推注疗法。分析动脉血压波形的随机森林机器学习 (ML) 模型预测液体反应性,比脉压变化等传统方法更准确
提高医务人员效率
- 基于 AI 的深度学习框架,例如卷积神经网络 (CNN) 与对比学习相结合,提高了对心律失常误报的检测,误报准确率达到 86%,真警报准确率达到 96%
- 用于机械呼吸机的闭环系统可以通过提供基于特定血流动力学目标的实时反馈来优化机械支持,例如心肺复苏,以改善结果
1.2 基于人工智能技术的心血管疾病防控研究进展
2025年02月10日 18:02 文章链接
AI 赋能心血管疾病早期预测和精准诊断
- 麻省理工学院 Caroline Uhler 团队利用 UK Biobank 数据库提出的跨模态自编码器框架可以整合心脏核磁和心电图双模态数据,全面表示心血管状态,提高心血管疾病相关表型预测的准确性
- 蒙特利尔心脏研究所 Gilbert Jabbour 团队开发并测试了ECG-AI模型,可以在窦性心律心电图的基础上预测新发心房颤动的风险,模型在总体患者和不同疾病亚组中均表现出良好的AF预测效能,且优于临床模型和心房颤动多基因评分
- 清华大学季向阳团队使用非接触式面部红外热成像信息进行冠状动脉疾病无创、快速、精准预测,性能优于国际指南推荐的验前概率模型(AUC 0.804 VS 0.713)
- Cedars-Sinai医学中心Damini Dey团队基于SCOT-HEART研究的1750名患者的影像组学分析发现基于CCTA的特异性影像组学特征在调整心血管风险评分和斑块负荷指标后与未来心肌梗死的发生显著相关
- 中国医学科学院赵世华团队开发并验证了一种用于自动化、计算机化心脏核磁的解读和诊断的深度学习方法,并对9719例患者的11种心血管疾病进行筛查和诊断
AI 赋能心血管疾病风险分层
- ORFAN研究纳入了8家英国医院的40991名患者,评估了FAI评分在有或无阻塞性冠心病情况下的预后价值,同时评估了一种集成了FAI评分、冠脉斑块指标和临床风险因素的智能化心血管事件风险预测算法
- AI-QCT模型与Diamond Forrester模型对阻塞性冠心病的累计发病率曲线显示随着风险分组的增加,累积发病率逐渐上升
- 帝国理工学院Fu Siong Ng团队发表了基于AI的心电图风险评估平台——AIRE平台。该平台在BIDMC内部队列中能从单导联心电图中生成患者特定生存曲线预测全因死亡率(C-index为0.775),并在
- 美国梅奥诊所Jae K Oh团队也发表了基于评估左室舒张功能障碍和充盈压升高的AI-ECG模型在中重度二尖瓣反流患者预后分层作用的研究
基于医学 AI 大模型的的心血管疾病早期预警、精准诊断和风险评估
- 上海交通大学刘成良团队提出了基于心电图的诊断大模型——KED模型,该模型根据80万份来自不同国家地区的患者心电图进行训练,并在中国、美国和其他地区的泛年龄段人群的心电图形态异常、节律异常、传导阻滞、房室肥大、心肌缺血和心肌梗死等疾病中显示出了极高的诊断精度
- 华中科技大学同济医院杨晓云团队通过对93824名患者的112685份心电图大数据进行深度神经网络学习,开发了心电图-Cor-Net模型。该模型可以提取与心血管疾病相关的心电波形特征,用于揭示所隐藏的心室肥大、扩大病理信息,诊断平均准确率达85.1%
- 韩国延世大学医学院Changho Han团队借助UK Biobank和KoGES两大数据库,首次系统评估了 ChatGPT 等大语言模型预测10年心血管疾病风险的能力,大模型的风险评估能力超过了传统 Framingham 风险评分
基于医学 AI 大模型的心血管疾病诊疗流程优化
- RAPID×AI 试验表明 AI 辅助决策在减少心血管事件的发生率方面具有显著性效果
- PROTEUS 试验发现AI辅助决策组转诊进行冠脉造影检查的AUROC为0.91;95%CI: 0.87-0.96),显著高于标准临床决策组(AUROC: 0.87;95%CI: 0.82-0.93)
- TeleTAVI 研究提示基于AI的远程随访可应用于绝大多数TAVI术后并发症风险较高患者的临床监测,且获得了较高的患者满意度
未来发展趋势:1)多模态数据深度融合与精准医疗;2)医学 AI 大模型的标准化和数据共享;3)强化学习与自适应 AI 系统;4)AI 与可穿戴设备及远程医疗深度结合;5)AI 辅助手术机器人的发展;6)伦理与监管体系完善
1.3 人工智能在麻醉学领域的应用进展
2025年02月25日 06:58 文章链接
术前麻醉风险评估
- 基于机器学习的髋关节修复手术术前自动化风险评估系统,术前根据人口学资料、基础疾病等22个特征,评估患者围手术期发生不良事件(死亡、急性心肌梗死、卒中、呼吸系统衰竭、肝肾功能衰竭和败血症)、术后入住重症监护治疗病房、住院时间延长等的相关风险
- 一种快速、无创且高度准确的深度学习算法,帮助麻醉医师术前预测困难气道的有效工具;对1000例全麻患者从9个不同的角度拍摄面部图像,采集下颌活动度、最大张口度、甲颌间距、Mallampati分级、头颈部运动和胸颌间距等特征,建立困难气道AI预测模型。AUC为0.943 5,敏感度89.58%,特异度90.13%
- 研究在甲状腺手术中预测困难气道的可行性,由机器学习中的平均算法确定的前5个困难气道危险因素分别为年龄、性别、体重、身高和体重指数,结果发现10种算法中梯度增强算法总体表现最好,AUC值为0.848,准确度为91.3%,精密度为100%
- 入1 160例全麻手术患者,收集包含12个音节在内的语音样本,提取共振峰和带宽特征;采用logistic回归分析声学参数与困难面罩通气之间的相关性;结果发现,困难面罩通气发生率为18.8%,逐步回归模型的AUC为0.779,敏感度和特异度分别为75.0%和71.0%
术中引导麻醉操作
- 肥胖及老年患者等特殊人群的解剖结构相对复杂、难以辨别,AI的机器学习算法能够对图像数据进行深入分析,自动识别关键解剖标志(如血管、神经以及穿刺目标区域)
- 基于U‑Net架构的深度学习,ScanNav外周神经阻滞超声系统通过超声影像实时识别93.5%的超声引导区域的重要解剖结构(叠加实时动态彩色影),并降低81.2%的超声引导阻滞失败的风险
- 智能麻醉穿刺辅助机器人系统,将超声影像与机器人、AI技术相结合,帮助年轻医师寻找穿刺靶点,同时通过机器人手臂辅助医师完成精准注射,为医师提供辅助穿刺及导航服务,减轻麻醉医师的负担
- 开普勒插管系统由一个操纵杆、一台作为“电子大脑”的计算机、一个碳纤维机械臂和一个连接可视喉镜等部件组成,将可视喉镜放置于正确位置,推动操纵杆即可插入气管导管;采用机器学习算法识别声门的敏感度和特异度分别为70%和90%,有望应用到商用可视喉镜中
术中麻醉深度检测
- 脑电双频指数(bispectral index, BIS)通过分析患者大脑电活动来反映患者的意识水平,BIS在40~60通常被认为是适合手术的麻醉深度;AI可以通过分析脑电图、心率变异性等更为复杂的生理信号,实现对麻醉深度实时且更为精确的监测
- 堆叠自动编码器‑长短期记忆(stacked deep auto‑encoder‑long short term memory, SDAE‑LSTM)使用预测概率(prediction probability, Pk)来测算脑电图与药物作用位点浓度之间的相关性,进而检验麻醉深度监测方法的效能。结果显示,SDAE‑LSTM 网络的Pk值为0.855,其准确率高于传统方法
术中血流动力学监测
- Hatib 等根据 1 344 例患者的动脉压数据开发了机器学习算法,能够在低血压发生前几分钟进行预测。该算法经过内部和外部验证,敏感度和特异度分别为88%和87%
- 基于机器学习的早期预警系统,从动脉压力波形中提取23个变量测算低血压预测指数,当指数在50~85时,系统建议麻醉医师引起注意并诊断发生原因,当指数>85时,系统综合患者心排血量、每搏量等指标给出治疗方案,要求麻醉医师在2 min内根据方案进行干预
- 估血容量状态(blood volume status, BVS)或失血严重程度的模型,采用穿戴式设备监测光电容积脉搏波描记、心震图和心电图,最终敏感度、特异度和AUC则分别为0.75、0.90和0.91
术中闭环靶控输注
- 丙泊酚TCI系统,以丙泊酚的药代动力学模型为基础,以听觉诱发电位指数(auditory evoked potential index, AEPI)为反馈变量,用比例‑积分‑微分闭环控制算法计算注射给药曲线
- 卷积神经网络模型“AI麻醉医师”,通过计算美国麻醉医师协会分级、年龄、身高、体重、性别、平均动脉压等数据提供用药建议并实时调控
术后远期随访
- AI技术能够实时分析可穿戴电子设备数据(体温、心电图、心率和血氧饱和度等),识别出心动过速、低血压以及新近发热等情况并立即通知专业医疗团队
- Mišić等的模型还可有效预测术后患者再入院率,Mamlook等的模型在预测手术部位感染方面的准确率达0.851 8,Ren等的模型在预测术后急性肾损伤、心血管并发症和神经系统并发症等方面表现良好,并能够将预测结果实时传输到医师的移动设备上
1.4 精准肿瘤学 :AI 的十大贡献 | 综述
2025 年 03 月 17 日 11:30 文章链接
AI 助力精准肿瘤学发展的十个领域:
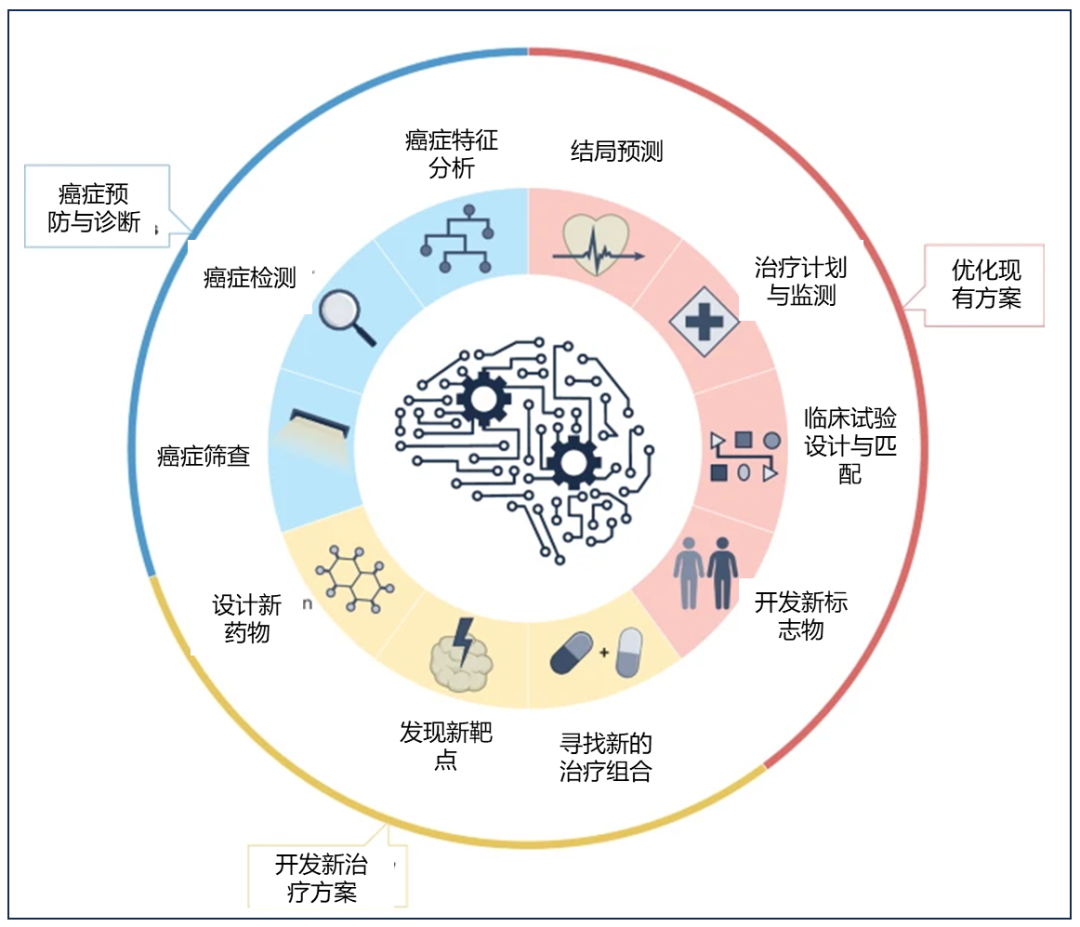
主要利益相关者团体之间开展合作,以推动人工智能技术造福患者:
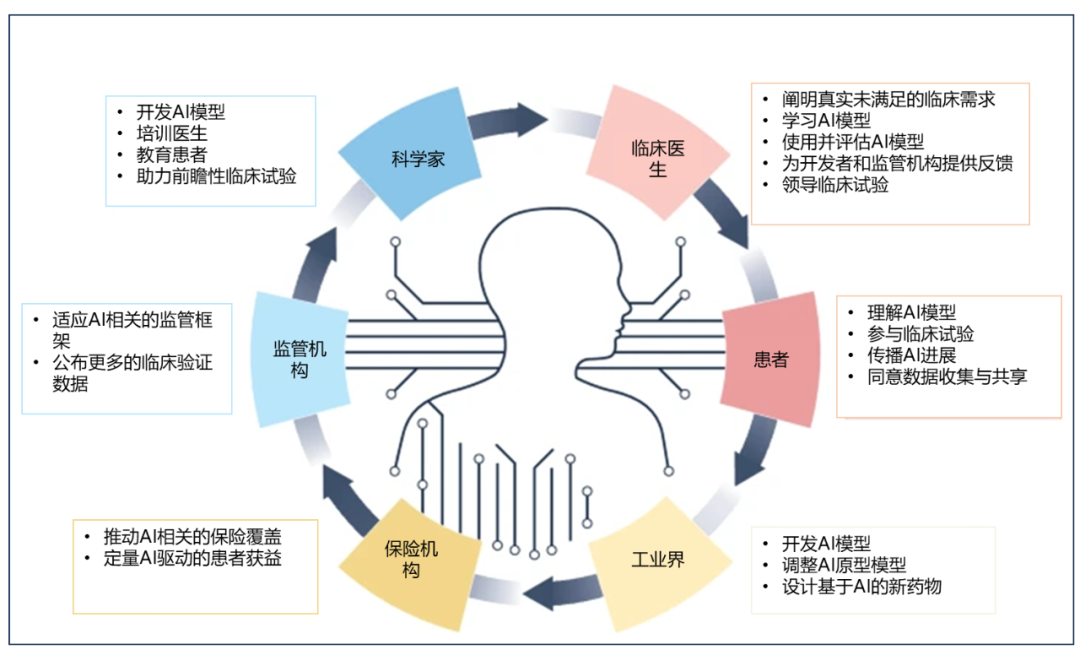
2 疾病监测
2.1 年至 2021 年中国贫困县 6 个月至 23 个月婴儿的营养不良
2025 年 03 月 文章链接
数据说明:
- 2016年至2021年在19个省的,针对832个最贫困的县每年连续进行六次横断面调查
- 多阶段集群抽样程序共选取了210,088名参与者;所有参与者都是6-23个月大的婴儿
主要结果:
- 2016年,四种主要营养不良形式普遍存在:贫血(流行率18.3%)、发育迟缓(7.5%)、消瘦(4.7%)和超重(3.1%)。任何两种共存的营养不良形式的流行率都很低。
- 从2016年到2021年,所有四种营养不良形式都减少了。贫血减少了 50% 以上,年减少率为9.11%(95% CI 4.83%~13.20%)。发育迟滞减少了 33% 以上,年降低率为10.44%(7.56%~13.22%)
- 母亲完成小学教育的婴儿患发育迟慢(调整后的 RR 为2.29,1.87~2.81)和消瘦(1.73,1.40~2.13)的风险大约是母亲具有大学或以上学历的儿童的两倍
- 男孩的生长较差和贫血较高。在所有结果中,与性别和教育相关的差异在6个月大时最大
与教育相关的婴儿成长不平等现象依然存在,这些差异尤其影响到那些母亲仅完成小学教育的儿童
3 模型预测
3.1 基于机器学习算法构建胸科患者术后并发症的预测模型
2025 年 02 月 18 日 06:58 文章链接
数据:
- 北京大学第一医院胸外科868例胸科手术患者数据
- 纳入标准:18~80岁、临床诊断为肺癌、拟行根治性外科切除手术并同意使用术后镇痛泵
- 排除标准:术前行放疗或化疗及免疫治疗、已存在远处或其他器官转移,合并自身免疫系统疾病、长期使用糖皮质激素以及1年内进行免疫抑制治疗,合并严重神经系统疾病、严重肝功能损害(Child‑Pugh classification C级)、肾衰竭(血肌酐值≥442 μmol/L)或正在进行肾脏替代治疗,美国麻醉医师协会(ASA)分级≥Ⅳ级,1年内有麻醉/手术史,存在硬膜外麻醉禁忌情况以及对局麻药过敏
- 术中的麻醉管理目标:维持脑电双频指数在40~60,必要时可使用血管活性药物,维持患者血压、心率的波动幅度在基础值的±20%,体温36 ℃~37 ℃,每搏量变异度≤13%
变量:
- 术前资料包括24项:性别、年龄、体重指数、吸烟史、饮酒史、是否术前合并疾病(慢性阻塞性肺疾病、哮喘、高血压病、2型糖尿病、脑卒中、短暂性脑缺血、心律失常、甲状腺疾病、肾功能不全)、肺功能相关指标{包括第1秒用力呼气量(FEV1)、第1秒用力呼气量占预计值的百分比(FEV1%)、1秒率[FEV1/用力肺活量(FVC)]、最大分钟通气量(MVV)}、血红蛋白水平、白蛋白水平、肌酐值、动脉血氧分压、动脉血二氧化碳分压、ASA分级。
- 术中资料包括19项:围手术期预防性吸入戊乙奎醚,麻醉方式(是否复合区域阻滞),术中是否使用一氧化二氮(N2O),术中是否使用七氟醚,术中是否使用右美托咪定,术中舒芬太尼剂量,术中舒芬太尼等效剂量,术中液体输入量,术中出血量,术中尿量,是否输血,术中是否出现低血压、高血压、新发心律失常,手术时长,手术方式(胸腔镜辅助或开胸手术),手术种类(肺部、胃/食管、纵隔),术后是否进入ICU,术毕是否拔除气管导管。
- 术后资料的收集:术后第1~3天,由课题随访人员床旁随访患者,用数字分级评分法(NRS)评分评估静息及运动疼痛,并收集血液检查结果。ICU患者常规每日抽血化验,转回普通病房的患者在术后第2天、第4~6天进行两次抽血化验,内容包括血常规、肝肾功能、心肌酶谱、心房钠尿肽。术后第2天常规进行胸部X线片检查,必要时由外科医师开具胸部CT检查。根据临床及检验检查结果判断是否有术后并发症的发生。
结局指标:术后并发症定义为术后新发的、对患者术后恢复存在不良影响的术后事件,主要包括有肺部并发症[包含肺炎、肺不张、肺栓塞、呼吸衰竭(机械通气时长>48 h)]、心血管并发症[新发心房扑动(房扑)/心房纤颤(房颤)、心肌损伤、急性心功能不全]、急性肾损伤、术后脑梗死、谵妄、外科并发症(肺漏、乳糜胸、术后出血需要二次手术),相应定义标准参考文献。此外,记录患者术后病理结果(恶性肿瘤或非恶性肿瘤)和住院时长
实验结论:
- 6 个机器学习模型,最优的是正则化回归(Glmnet)算法下的AUC为0.773(95%CI 0.746~0.779),准确率为0.765(95%CI 0.721~0.778),校准度为0.165(95%CI 0.158~0.182)
- 前10位变量依次是手术时间长、围手术期未预防性吸入戊乙奎醚、性别为男性、术后第3天运动NRS评分高、术后进入ICU、手术种类为胃/食管、MVV低、术中舒芬太尼等效剂量大、年龄高、术中出血量大
4 治疗干预
4.1 人工智能有利于 ICU 的血流动力学管理
2024 年 12 月 30 日 12:58 文章链接
血流动力学监测优化:
- 基于 AI 的热成像可以预测休克,仅在必要时进行接触或侵入性监测
- 分析单导联心电图数据的 DNN 可以检测升高的左心房压并估计左心室射血分数。
- AI 驱动的脉搏轮廓分析从动脉波形中提取每搏输出量 (SV),性能优于传统方法
- 根据血压、近红外光谱 (NIRS) 脑氧合和经颅多普勒 (TCD) 血流速度等数据训练的支持向量机在预测低血容量方面显示出前景,其中 TCD 的特异性最高
- 低血压预测指数 (HPI) 等算法可以通过分析动脉波形来预测低血压,
血流动力学状况的分类或特征:
- AI 有助于对患者和疾病进行分类,例如区分动脉颤动和窦性心律
- AI 模型甚至可以预测心律失常的发作,为先发制人的干预铺平道路
- AI 模型用血压波形可以高精度无创地检测到主动脉瓣狭窄 (AoS)
- 分层聚类确定了 6 种不同的术中低血压内型,为个性化治疗提供了见解
血流动力学状况的治疗或效率改善:
- 血流动力学稳定指数 (HSI) 通过分析 ICU 数据来预测重症患者的不稳定情况,AUC 为 0.82,特异性为 92%;HSI 还能提供置信区间和特征重要性
- 分析动脉血压波形的随机森林机器学习 (ML) 模型预测液体反应性,比脉压变化等传统方法更准确,可用于个体化液体管理
- 卷积神经网络 (CNN) 与对比学习相结合,提高了对 ICU 中假的心律失常的误报检测,误报准确率达到 86%,真警报准确率达到 96%
- 基于特定血流动力学目标的实时反馈来优化机械支持,例如心肺复苏
4.2 麻醉深度对中老年全麻患者心率变异性和血流动力学的影响
2025 年 02 月 03 日 06:02 文章链接
心率变异性(HRV):衡量连续心动周期长度变化的指标,反映了自主神经系统对心率的调节情况
实验设计:
- 选取了111例接受硬膜外麻醉联合全麻治疗的胃癌患者作为研究对象,并随机分为 3 组
- 通过调整麻醉药物的输注速度,维持各组患者的双谱指数(BIS)在特定范围:A 组 BIS 维持在50-59,B 组 BIS 维持在40-49,C 组 BIS 维持在30-39
- 血液动力学参数:高频功率(HFP)、低频功率(LFP)、总功率(TP)、平均动脉压(MAP)、心率(HR)、舒张压(DBP)以及收缩压(SBP)等
- 血液动力学参数记录时间:麻醉诱导前(T1)、插管后(T2)、插管后3分钟(T3)以及拔管后6分钟(T4)
实验结论:
- 维持较低的麻醉深度(BIS 40-49)对中老年全麻患者的心率变异性和血流动力学具有积极影响;在此麻醉深度范围内的患者展现出更快的自主呼吸恢复、更短的睁眼时间以及更快的拔管时间,同时并未增加不良反应的发生率